近年来的研究表明,带电界面在水环境中能够自发形成电双层,该结构由静电场、溶剂偶极取向、离子不对称分布及界面富集等效应共同构建,可显著调控界面电子转移与氧化还原化学反应。这一现象不仅存在于传统电极材料中,也广泛出现在软物质体系,如蛋白质相分离形成的凝聚体、淀粉样肽等生物材料的表面。这些生物界面虽无外加电压,却因热力学势梯度(如水分子偶极排列或相变引起的溶剂密度梯度)而产生内建电势,类似于法拉第所描述的“蒸汽电”过程。然而,尽管这类界面已被证实具备驱动非均相氧化还原反应的潜力,如何主动设计和调控软生物材料的界面电化学微环境,以可控地生成电子并驱动特定化学反应,仍是尚未实现的关键挑战。
二、【创新成果】
基于以上难题,美国圣路易斯华盛顿大学代怡帆博士在Nature Materials上发表了题为“Electrogenic protein condensates as intracellular electrochemical reactors”的论文,报道通过基因编码设计并能自组装成蛋白质凝聚体的生物材料,可被工程化设计为电化学反应器。研究人员揭示了决定蛋白质凝聚体序列-电化学性质关系的基本原理,从而实现了对其产电行为的程序化调控,随后在体外验证了这类蛋白质凝聚体在多种电化学反应中的应用。此外,研究人员还将这些凝聚体作为“活体材料”应用于活细胞内,实现了细胞内纳米颗粒合成、污染物降解以及通过人工铁死亡机制实现无抗生素抑菌。这类具有本征电活性的材料为开发下一代生物电化学器件提供了一个清洁、可持续的生物材料平台,有望成为新型能源来源。

三、【图文解析】
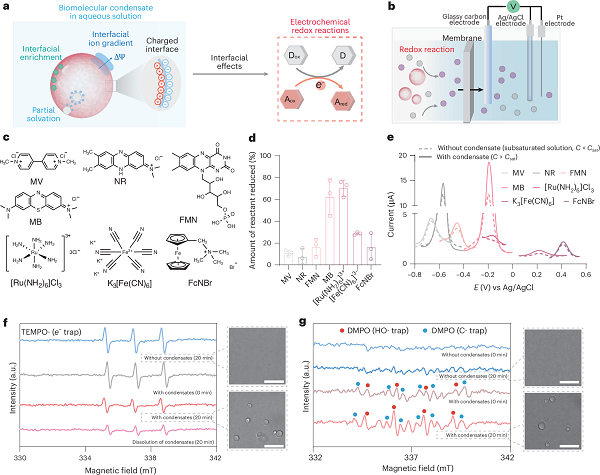
图1 电活性蛋白质凝聚体的电化学氧化还原活性 © 2026 Springer Nature
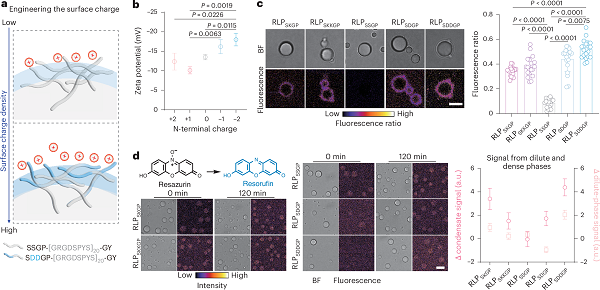
图2 通过调控凝聚体的表面电荷状态以增强其还原活性 © 2026 Springer Nature
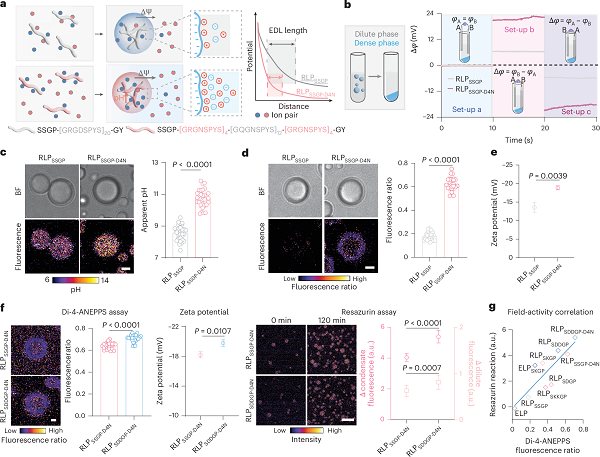
图3 通过编程调控相变中的不对称性以增强界面电化学活性 © 2026 Springer Nature
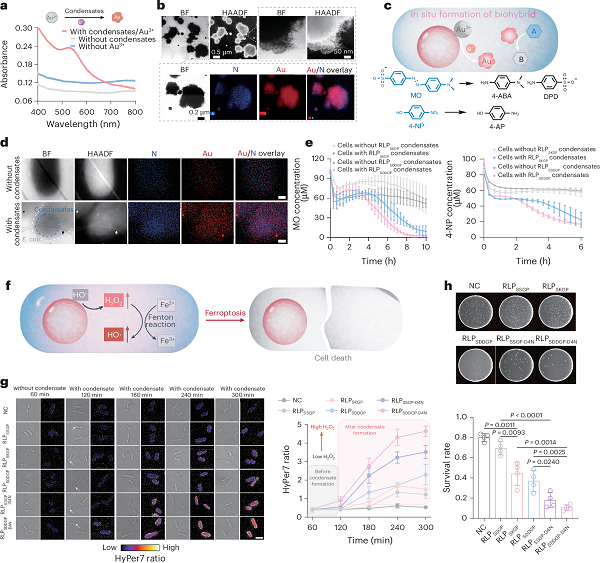
图4 电活性蛋白质凝聚体作为细胞内电化学反应器 © 2026 Springer Nature
四、【科学启迪】
综上,本研究揭示了由内在无序蛋白相变形成的微米级蛋白质凝聚体可自发建立界面电势梯度,具备可编程的电化学活性。其活性由表面氨基酸残基和相变不对称性决定,但离子不对称产生电势的机制仍待阐明。研究检测到羟基自由基,提示界面氢氧根参与电子转移,未来需解析电子供受体网络及传递路径,以定向调控还原反应。该工作首次构建了完全基于生物分子、可在活细胞内运行的电活性平台,通过基因编码实现纳米合成、污染物降解和人工铁死亡等应用,开创了“活体电化学材料”新范式,为细胞尺度的可持续电化学工程提供了全新策略。
原文详情:Electrogenic protein condensates as intracellular electrochemical reactors (Nat. Mater., 2026, DOI: 10.1038/s41563-025-02434-0)
本文由赛恩斯供稿。