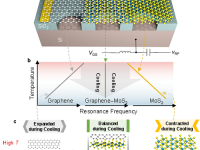
有机化学新突破:该篇Science实现Z选择性C-H官能团化
一、【科学背景】
C-H键的转化是有机合成领域长期以来的目标。数十年的研究已开发出多种机理各异的策略,将这类传统惰性键替换为新的C-C键。在此广阔领域中,控制立体选择性的策略至关重要。尽管近期出现了一些C-H官能团化反应的实例,但Z选择性烯基C-H官能团化反应仍难以实现。例如,尽管诺贝尔奖获奖反应—赫克反应已历经半个多世纪的创新,但其Z选择性变体仍未出现。尽管已知存在其他合成Z-烯烃的策略,但所有选择性断裂亲Z-C-H键的方法均依赖导向基实现立体选择性。这种策略本质上将Z-选择性C-H官能团化局限于一小类带有强配位辅助基的刚性烯烃。总之,要实现非导向性Z选择性C-H官能团化的互补方法,必须建立新的机理策略以克服阻碍Z烯烃形成的固有热力学障碍。
二、【创新成果】
基于上述挑战,近期威斯康星大学麦迪逊分校Zachary K. Wickens教授、加州大学洛杉矶分校Osvaldo Gutierrez教授、Marcel Schreier教授团队构想了一种根本不同的Z选择性C-H官能团化方法。具体而言,通过将末端烯烃转化为瞬态1,2-双去核体,随后进行Z选择性消除反应,即可获得Z-烯基枢纽(图1B)。这一看似简单的方案需要通过立体选择性消除反应生成Z-1,2-二取代烯烃。遗憾的是,这一看似基础的反应需违背有机化学入门课程的基本法则:E2反应的立体选择性由能发生反式消除反应的最小立体位阻纽曼投影决定。事实上,尽管二卤化物等双核受体可轻易由末端烯烃制备,但其消除反应必然生成预期的E-烯基卤化物及支链产物。因此,在本文中,该研究团队提出一种基于独特Z选择性脱离反应的Z选择性C-H官能团化策略。该方法通过将烯烃转化为瞬态1,2-双噻蒽鎓双亲核体,使其在亲Z过渡态中通过稳定作用克服空间位阻,从而颠覆了沿用七十年的E2立体选择性模型。
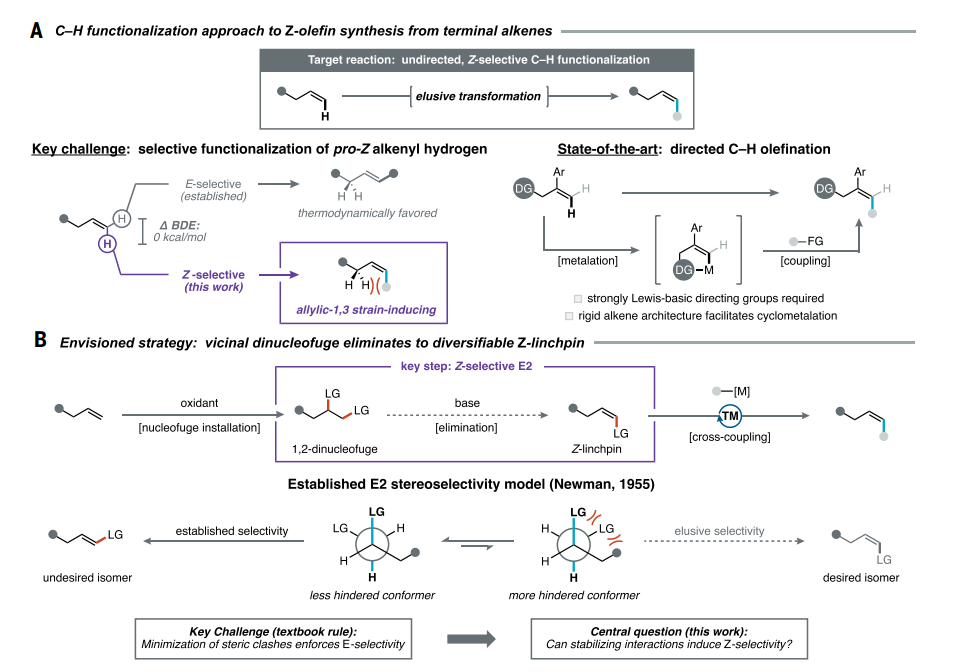
图1 该项工作的概述;© 2025 Science
在研究噻蒽(TT)与烯烃形成的双加成物与单加成物的电化学反应性时,研究人员观察到双加成物与单加成物的摩尔比与生成的脱去产物中Z-E异构体比例存在明确对应关系(图2A)。该趋势预示双加成物将选择性脱去生成Z-烯基硫蒽鎓产物1。为验证此预测,研究人员分离出电解生成的微量双加成物,并用弱碱三氟乙酸盐(该试剂不会促进烯基硫蒽鎓异构化)进行处理。实验证实双加成物以近乎完美的Z选择性发生脱去反应,该发现为建立Z选择性C-H官能团化通用策略奠定了基础。
随后,研究人员设计的电化学系统,同时抑制了单加成反应并防止双加成向单加成的转化。虽然最初采用分隔电解池以维持高法拉第效率,但研究人员设想使用无分隔电解池—即在反应室中引入阴极,这可带来两大优势(图2C)。首先,阴极通过还原阳极可维持TT的高稳态浓度,从而抑制歧化反应,在无需大量过量TT的情况下减少单体生成。其次,阴极上三氟乙酸的氢析出反应将生成三氟乙酸盐碱。这种配对电解装置确保仅在形成加合物时产生碱,从而缓解碱诱导的反应抑制。研究人员发现未分隔电解池颠覆了噻蒽化反应的典型立体选择性,在极少额外优化下即以高收率和Z选择性获得模型烯基噻蒽鎓盐1(图2D)。
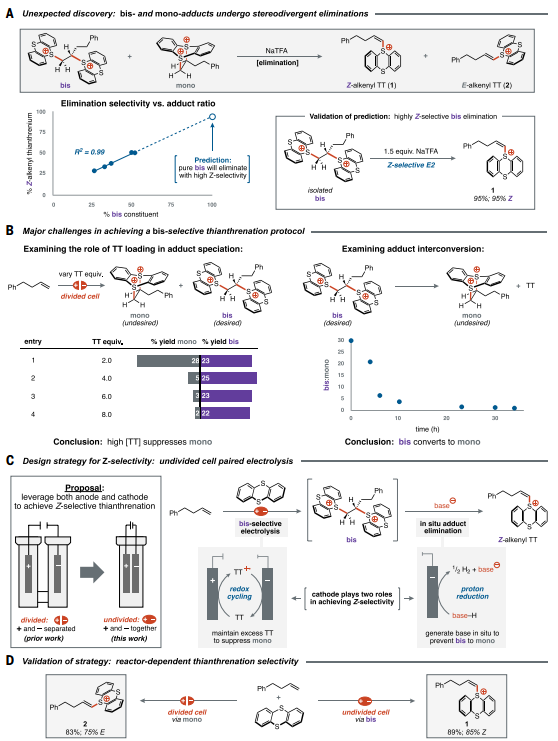
图2 反应设计;© 2025 Science
随后,研究人员探究了适用于该Z选择性噻蒽化反应的烯烃范围(图3A)。在整个研究过程中,他们发现该过程的固有Z选择性始终保持在较高水平。此外,这些Z-烯基噻蒽鎓盐具有卓越的结晶性,通过重结晶可获得近乎对映体纯的产物。这相较于传统烯烃合成具有显著优势,在未分隔的反应池条件下,通过含多种常见官能团的末端烯烃,可轻松获得Z-烯基硫蒽鎓盐。其他含亲核性官能团的烯烃底物,如酰胺、羧酸和磺酰胺,均可在不经原位转化情况下实现噻蒽化。
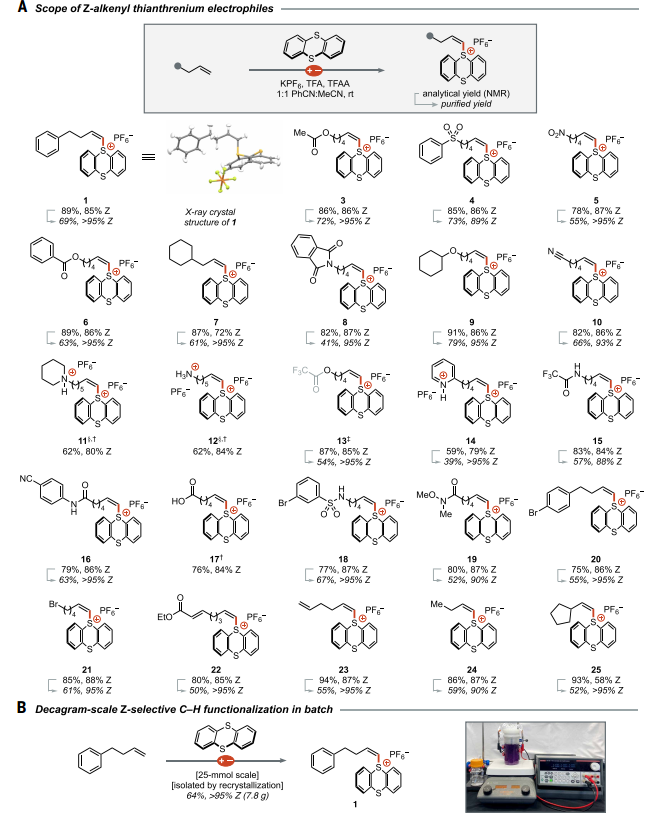
图3 Z-选择性C–H噻蒽化反应; © 2025 Science
进一步地,该研究团队展示了该类Z型烯基硫蒽鎓盐在多种交叉偶联反应中的适用性,Sonogashira、Suzuki、Negishi、Heck偶联以及羰基化反应在内的一系列反应,均能高度保持烯烃的Z构型。还方法还被成功应用于多种生物活性天然产物的合成中,特别是一些生物信息素(图4),显示出其强大的合成实用性和步骤经济性。
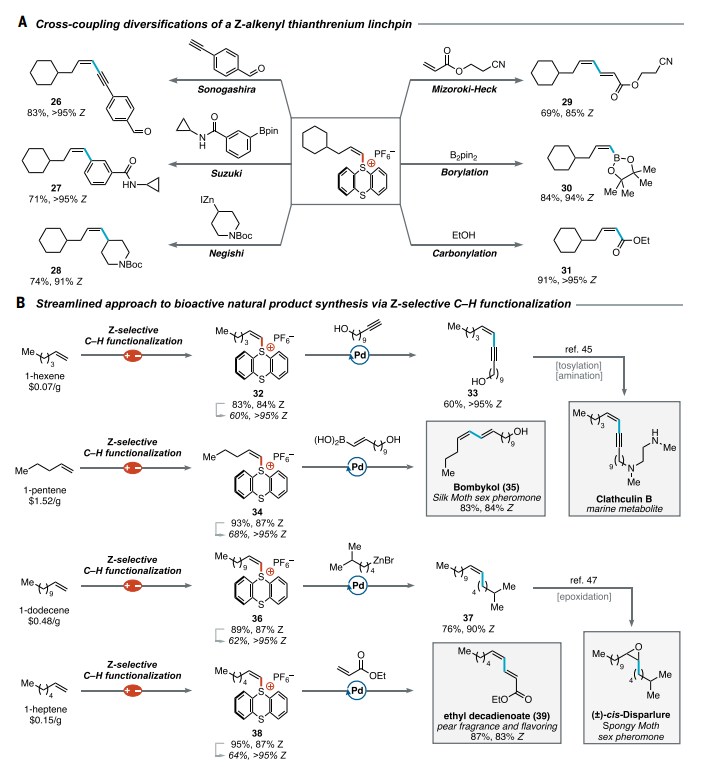
图4 合成应用; © 2025 Science
研究人员最后对该反应的机理进行了探究,基于计算化学分析,他们发现,虽然从基态构象上看,E型消除路径似乎更有优势,但在过渡态中,Z型路径因保留了关键的π-π堆叠和C-H···S氢键作用而能量更低。在维持关键稳定作用的同时,立体位阻最小的过渡态最终形成Z型立体异构体(图5C)。研究人员随后设计了将硫原子替换为氧原子的对照实验,进一步验证了氢键作用在立体控制中的关键角色。
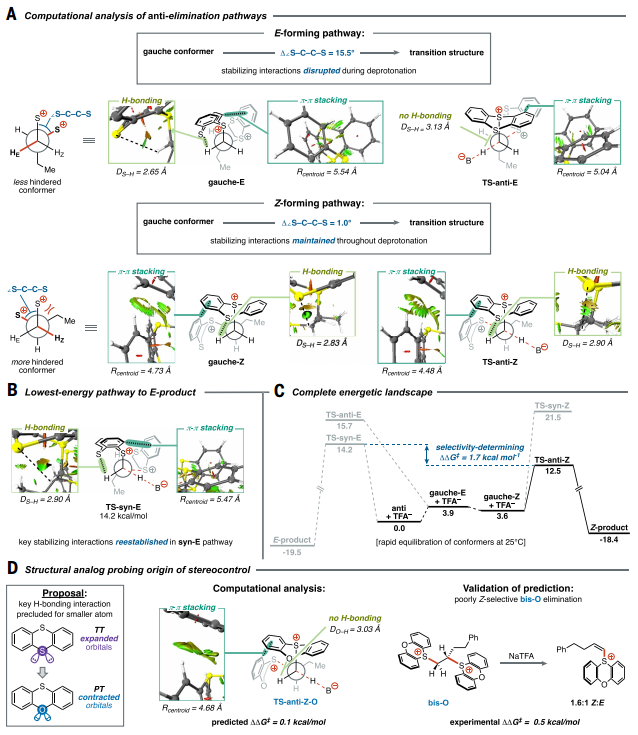
图5 Z-选择性的机理研究; © 2025 Science
该研究揭示了烯烃转化为瞬态1,2-双噻蒽鎓中间体的过程,该中间体通过稳定作用打破教科书式的E2立体选择性规则,实现Z选择性消除反应。研究发现成对电解既能选择性生成必需的双噻蒽鎓中间体,又能驱动其原位快速消除,成为实现该目标的关键策略。由此获得的Z式锚定体,通过稳健的交叉偶联反应,使廉价原料得以转化为多种目标Z-烯烃化合物。文章以“Stereo-reversed E2 unlocks Z-selective C–H functionalization”为题发表在国际顶级期刊Science上,引起了相关领域研究人员热议。

三、【科学启迪】
综上所述,该研究团队完成的这项研究为长期存在的难题提供了解决方案:实现未活化烯烃的Z-选择性C-H官能团化。该转化通过瞬态双噻蒽鎓中间体的意外Z-选择性脱离反应得以实现,该中间体通过稳定作用打破了教科书中关于E2反应立体选择性的预测。研究人员阐明了如何将电化学电池设计作为关键参数,既能选择性生成必需的双噻蒽鎓二核受体,又能驱动其原位快速脱去以规避其固有不稳定性。这项工作不仅为Z-烯烃合成提供了实用方法,更揭示了非共价相互作用如何在脱去反应中超越固有立体选择性,未来有着广阔的研究空间。
文献链接:Stereo-reversed E2 unlocks Z-selective C-H functionalization,2025,https://doi.org/ 10.1126/science.adv7630)
本文由LWB供稿。